末梢性免疫寛容のメカニズム解明に対しノーベル生理学・医学賞が授与される
作者: Dmitry Drozd

カロリンスカ研究所のノーベル委員会は、2025年のノーベル生理学・医学賞を、メアリー・E・ブランコウ氏、フレッド・ラムズデル氏、そして坂口志文氏の三氏に授与することを決定しました。彼らの画期的な発見は、「末梢性免疫寛容」という極めて重要なプロセスに関するものです。これは、免疫系が自身の組織を攻撃するのを防ぎ、自己免疫疾患から体を守る仕組みです。
歴史的背景と発見の経緯
免疫寛容、すなわち免疫系が有害な侵入者を標的としながら、自身の細胞を認識して攻撃を避ける能力は、75年以上にわたり研究されてきました。この分野の基礎は、1945年のレイ・D・オーウェン氏による初期の研究、そして1950年代のレスリー・ブレント氏、ルパート・ビリンガム氏、ピーター・メダワー氏らの業績によって築かれました。
これらの初期の洞察は、特定の条件下で免疫系が異質な組織を受け入れるように訓練され得ることを示しました。これにより、「中枢性寛容」という概念が確立されました。これは、自己反応性を持つ可能性のある免疫細胞が、胸腺での発達過程で排除されるメカニズムです。バーネット氏とメダワー氏は、この根本的な仕組みである「獲得免疫寛容の発見」により、1960年にノーベル賞を受賞しています。
しかしながら、中枢性寛容だけでは不完全であることが認識されていました。一部の自己反応性免疫細胞は、この排除プロセスをすり抜け、体内に循環し、自己免疫攻撃のリスクをもたらします。ブランコウ氏、ラムズデル氏、坂口氏の発見が、この理解のギャップを埋め、末梢性寛容の解明へとつながりました。
ブレークスルーとなった発見
多くの科学者が免疫寛容は中心的な細胞排除にのみ依存していると考えていた1995年、坂口志文氏が画期的な発見をしました。彼は、免疫細胞の新しいクラスである「制御性T細胞(Tregs)」を発見したのです。
Tregsは、自己抗原に対する免疫応答を積極的に抑制し、自己免疫疾患を予防する役割を果たします。これは、胸腺の外で免疫活動を監視する、洗練された末梢メカニズムの存在を明らかにするものでした。
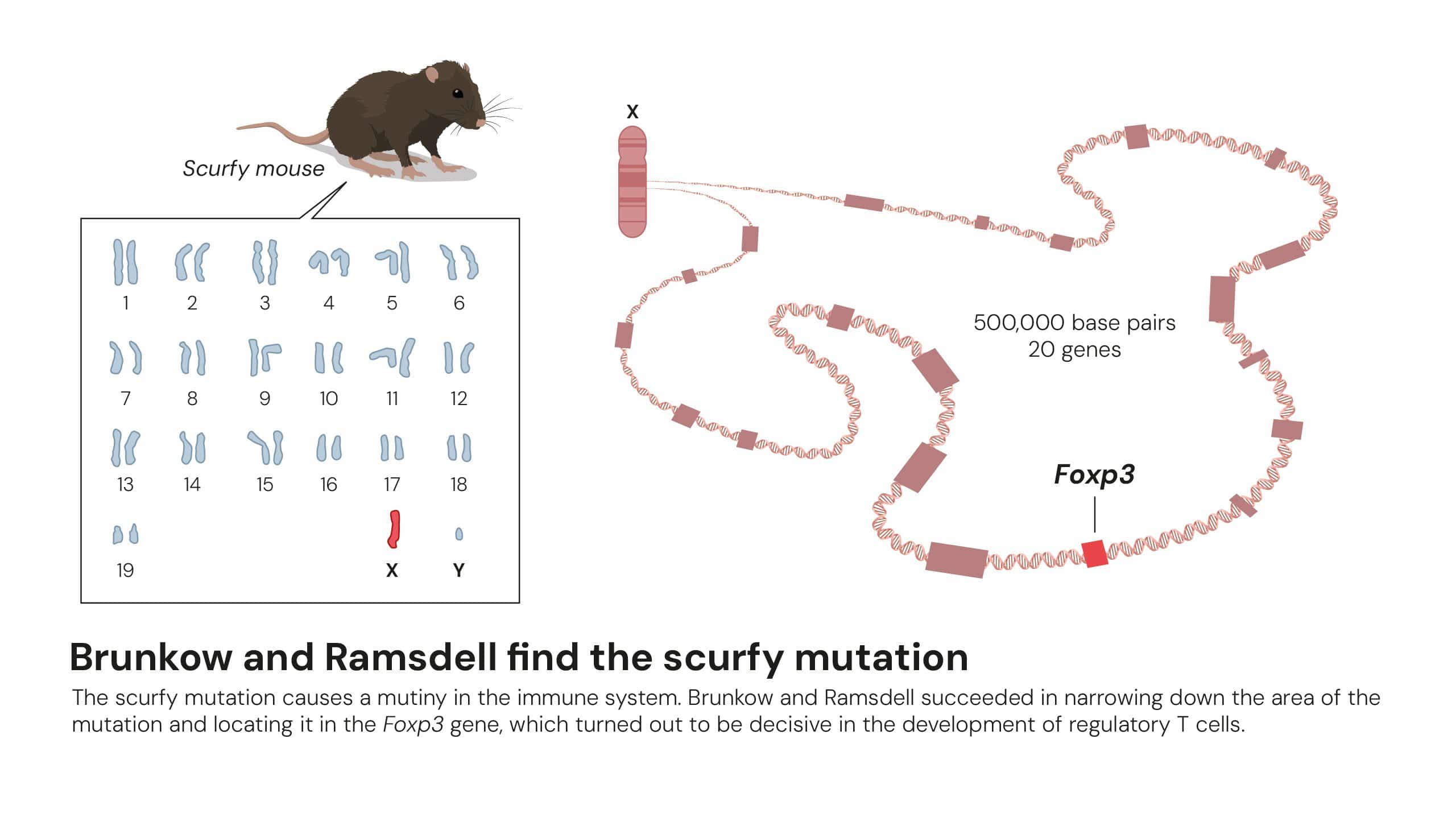
これを補完するように、2001年にメアリー・ブランコウ氏とフレッド・ラムズデル氏が共同で行った研究では、制御性T細胞の機能喪失と重度の自己免疫疾患感受性を引き起こすFoxp3遺伝子変異がマウスで特定されました。
さらに、彼らはヒトのFoxp3遺伝子の変異が、稀ではあるものの重篤なIPEX症候群に関連していることを確認し、この遺伝子が免疫調節において不可欠な役割を担っていることを裏付けました。その後、坂口氏はFoxp3が制御性T細胞の発達を制御していることを実証し、細胞レベルと遺伝子レベルの発見を結びつけ、末梢性免疫寛容の包括的な理解を確立しました。
末梢性免疫寛容がもたらす恩恵
免疫系は、毎日何千もの病原体から私たちを守る、並外れた力を持っています。しかし、この力は正確に制御されなければなりません。制御が失われると、免疫系は自身の組織を攻撃し、1型糖尿病、多発性硬化症、関節リウマチといった慢性的な、しばしば衰弱性の自己免疫疾患を引き起こします。
主に制御性T細胞によって媒介される末梢性免疫寛容は、この免疫活動に対する「重要なブレーキ」として機能し、自己寛容と免疫バランスを確保しています。
このメカニズムがなければ、臓器移植のような一般的な救命医療介入は免疫拒絶を引き起こし、多くの慢性自己免疫疾患は治療不可能となるでしょう。今回の受賞者たちの発見は、科学的理解を深めただけでなく、制御性T細胞を調節して癌と闘い、自己免疫疾患を予防し、移植の成績を向上させる治療法の革新を促しました。
これらの経路を標的とするいくつかの治療法は現在、臨床試験段階にあり、世界中の患者に希望をもたらしています。
ノーベル委員会の委員長であるオッレ・ケンペ氏は、「ブランコウ氏、ラムズデル氏、坂口氏の業績は、免疫系のバランスを維持する複雑かつ不可欠なメカニズムを明らかにし、変革をもたらしました。彼らの発見は、現代の免疫学と治療法の革新の基礎となっています」と強調しました。
免疫系が自己破壊することなく身体を保護するメカニズムを解明したことで、2025年のノーベル賞受賞者たちは、基礎生物学と医学の両方を劇的に進歩させ、自己免疫疾患、癌、および移植治療の改善に向けた希望を提供しました。
この受賞は、人間の健康を守る複雑な生物学的システムを解き明かす上で、基礎科学研究が持つ計り知れない価値を浮き彫りにしています。
45 ビュー
このトピックに関するさらに多くのニュースを読む:
エラーや不正確な情報を見つけましたか?できるだけ早くコメントを考慮します。

