2025年諾貝爾生理學或醫學獎揭曉:解鎖周邊免疫耐受機制
作者: Dmitry Drozd

卡羅林斯卡學院(Karolinska Institutet)的諾貝爾大會宣布,2025年諾貝爾生理學或醫學獎頒發給瑪麗·E·布倫科(Mary E. Brunkow)、弗雷德·拉姆斯戴爾(Fred Ramsdell)以及坂口志文(Shimon Sakaguchi),以表彰他們在周邊免疫耐受機制方面開創性的發現。這項機制至關重要,它能防止免疫系統攻擊自身的組織,從根本上避免了自體免疫疾病的發生。
免疫耐受的歷史脈絡與核心挑戰
免疫耐受現象,即免疫系統在識別並清除有害入侵者的同時,能夠寬容對待自身細胞的能力,已成為長達七十五年研究的核心課題。早在1945年,雷·D·歐文(Ray D. Owen)便展開了早期探索,隨後在1950年代,萊斯利·布倫特(Leslie Brent)、魯珀特·比林厄姆(Rupert Billingham)和彼得·梅達沃(Peter Medawar)的研究奠定了基礎,證明免疫系統在特定條件下可以被「訓練」以接受外來組織。這些見解催生了「中樞耐受」的概念,即潛在的自體反應性免疫細胞在胸腺發育過程中被清除。伯內特(Burnet)和梅達沃更因此項「獲得性免疫耐受的發現」,共同榮獲了1960年的諾貝爾獎。
然而,科學界逐漸認識到中樞耐受並非萬無一失。總有一些自體反應性免疫細胞會逃脫胸腺的篩選機制,並在體內循環,構成自體免疫攻擊的潛在風險。正是針對這個未解的難題,瑪麗·布倫科、弗雷德·拉姆斯戴爾和坂口志文三位科學家,透過他們對周邊耐受機制的突破性研究,成功填補了知識上的空白。
關鍵性的里程碑發現
在1995年,許多科學家仍堅信免疫耐受僅依賴於中樞對有害細胞的清除時,坂口志文教授卻發現了一種全新的免疫細胞類型——調節性T細胞(Regulatory T cells, Tregs)。這些細胞的主動功能是抑制針對自身抗原的免疫反應,從而有效預防自體免疫疾病。這項發現揭示了一個精密的周邊機制,證明免疫系統的活動監控並非只在胸腺內進行。
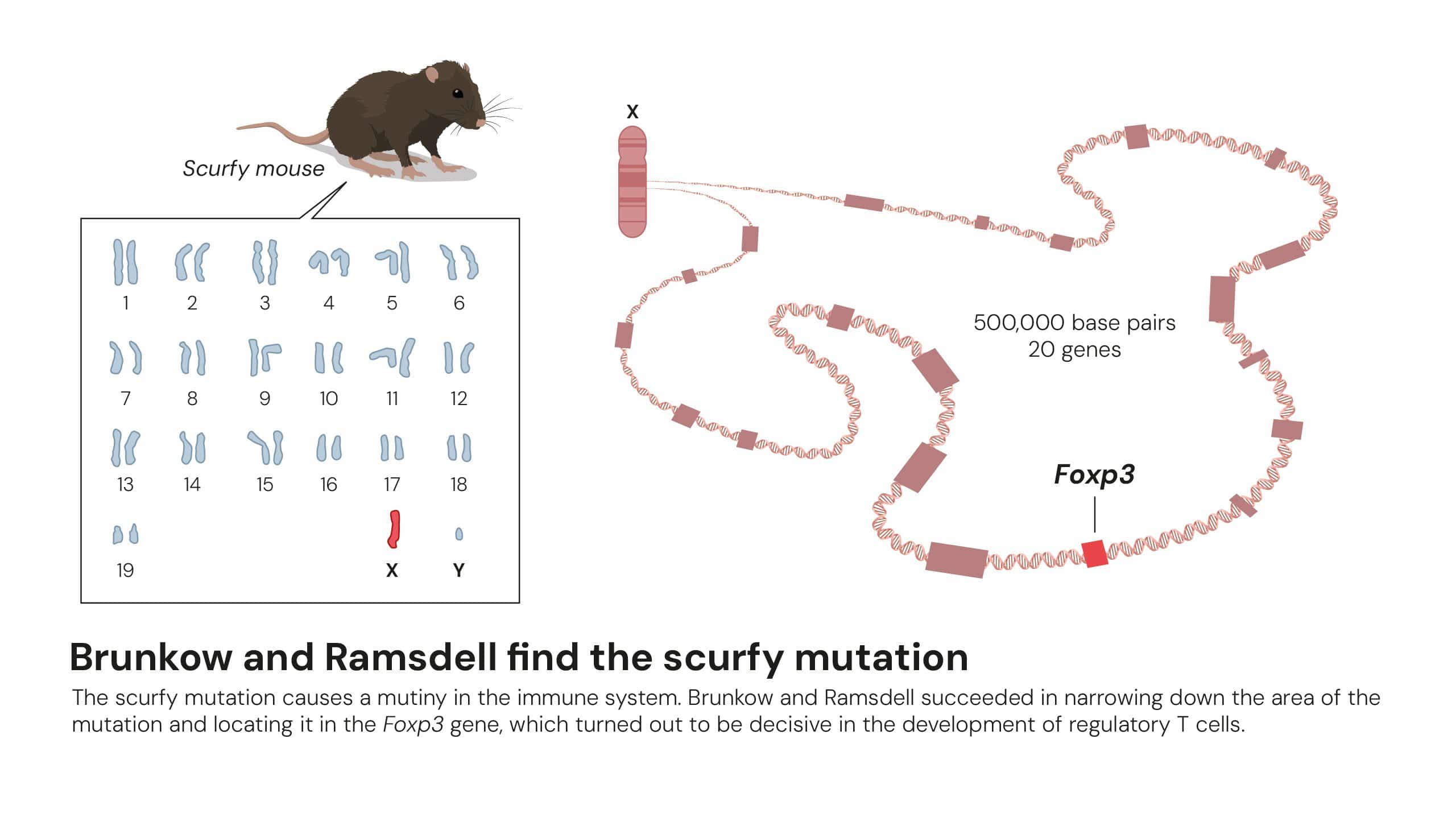
與此同時,瑪麗·布倫科和弗雷德·拉姆斯戴爾在2001年進行了互補性的研究。他們在小鼠體內發現了Foxp3基因突變會導致調節性T細胞功能喪失,進而引發嚴重的自體免疫疾病易感性。他們進一步確認人類Foxp3基因的突變與罕見但破壞性極強的IPEX綜合徵有關,從而確立了該基因在免疫調節中的核心地位。
隨後,坂口志文證明了Foxp3基因正是調節性T細胞發育的關鍵調控者。這項工作將遺傳學和細胞生物學的發現緊密地結合在一起,形成了一個關於周邊免疫耐受機制的完整且全面的理解。
周邊免疫耐受對人類健康的深遠影響
免疫系統的力量無比強大,它日復一日地保護我們免受數千種病原體的侵害。然而,這種力量必須受到精確的控制;否則,免疫系統可能會反噬自身組織,導致慢性且往往使人衰弱的自體免疫疾病,例如第一型糖尿病、多發性硬化症和類風濕性關節炎。周邊免疫耐受,主要由調節性T細胞介導,正是對免疫活動施加的關鍵「剎車」,確保了自體寬容和免疫平衡。
如果沒有這套精密的機制,許多挽救生命的醫療干預措施,例如器官移植,將會引發無可避免的免疫排斥反應,並且許多慢性自體免疫疾病也將束手無策。三位獲獎者的發現不僅深化了科學理解,更激發了治療學上的創新浪潮。這些創新包括調控調節性T細胞以對抗癌症、預防自體免疫疾病,以及改善移植手術的預後。
目前,數種針對這些通路的新型療法正在臨床試驗中進行測試,為全球的病患帶來了無限的希望與可能。
諾貝爾委員會主席奧勒·坎佩(Olle Kämpe)強調:「布倫科、拉姆斯戴爾和坂口志文的工作具有變革性,揭示了維持免疫系統平衡的複雜且必要的機制。他們的發現是現代免疫學和治療創新的基石。」
透過闡明免疫系統如何在保護身體的同時避免自我毀滅的機制,2025年諾貝爾獎得主們極大地推動了基礎生物學和醫學的發展,為自體免疫疾病、癌症和移植領域的治療帶來了改進的曙光。這項殊榮再次凸顯了基礎科學研究在揭示保障人類健康的複雜生物系統方面所具備的深遠價值。
45 浏览量
閱讀更多有關此主題的新聞:
发现错误或不准确的地方吗?我们会尽快处理您的评论。

