Le Prix Nobel de Physiologie ou Médecine 2025 récompense la découverte des mécanismes de tolérance immunitaire périphérique
Auteur : Dmitry Drozd

L'Assemblée Nobel de l'Institut Karolinska a décerné le Prix Nobel de physiologie ou médecine 2025 à Mary E. Brunkow, Fred Ramsdell et Shimon Sakaguchi. Ils sont honorés pour leurs découvertes fondamentales concernant la tolérance immunitaire périphérique. Ce processus est essentiel car il empêche le système immunitaire d'attaquer les propres tissus de l'organisme, offrant ainsi une protection vitale contre le développement des maladies auto-immunes.
Contexte Historique et Évolution de la Tolérance
La tolérance immunitaire, qui est la capacité du système de défense à reconnaître et à épargner les cellules de l'organisme tout en ciblant les envahisseurs nocifs, fait l'objet d'études approfondies depuis plus de 75 ans. Les travaux pionniers de Ray D. Owen en 1945, suivis par ceux de Leslie Brent, Rupert Billingham et Peter Medawar dans les années 1950, ont jeté les bases. Ils ont démontré que le système immunitaire pouvait être conditionné à accepter des tissus étrangers dans certaines circonstances.
Ces premières révélations ont conduit à l'établissement du concept de tolérance centrale. Selon ce principe, les cellules immunitaires potentiellement autoréactives sont éliminées pendant leur développement au sein du thymus. Burnet et Medawar avaient d’ailleurs reçu le prix Nobel en 1960 pour « la découverte de la tolérance immunitaire acquise », validant ainsi ce mécanisme fondamental.
Néanmoins, il est rapidement apparu que la tolérance centrale était imparfaite. Certaines cellules immunitaires autoréactives échappent à ce processus d'élimination et continuent de circuler dans le corps, ce qui crée un risque constant d'attaques auto-immunes. C'est précisément cette lacune dans la compréhension scientifique que Mary Brunkow, Fred Ramsdell et Shimon Sakaguchi ont comblée grâce à leurs travaux sur la tolérance périphérique.
Les Découvertes Majeures
En 1995, à une époque où de nombreux scientifiques croyaient que l'immunotolérance dépendait uniquement de l'élimination centrale des cellules dangereuses, Shimon Sakaguchi a réalisé une percée. Il a identifié une nouvelle catégorie de cellules immunitaires : les lymphocytes T régulateurs (Tregs). Ces cellules ont la capacité d'inhiber activement les réponses immunitaires dirigées contre les auto-antigènes et de prévenir les maladies auto-immunes, révélant un mécanisme périphérique sophistiqué qui surveille l'activité immunitaire en dehors du thymus.
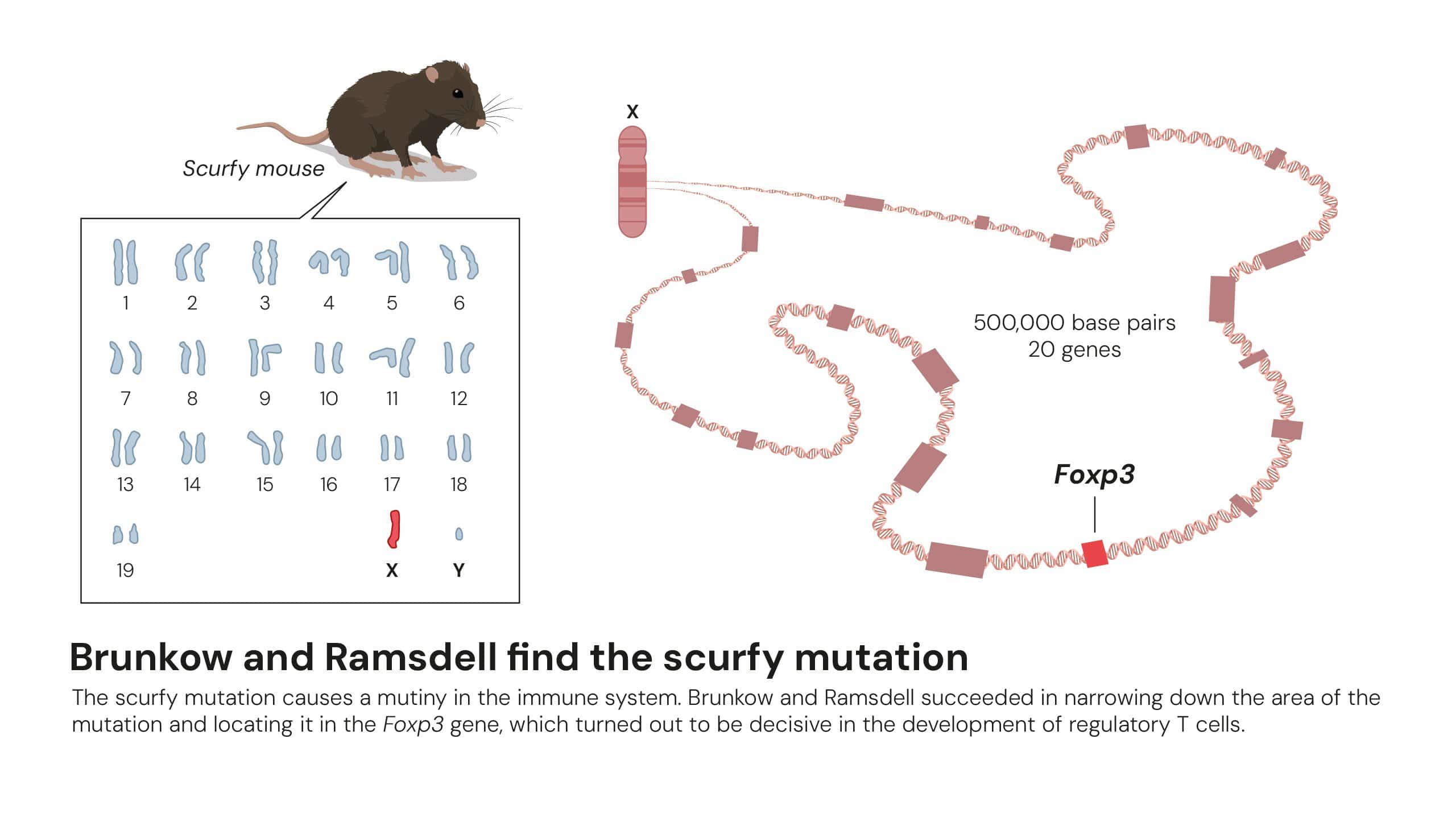
Les recherches complémentaires menées par Mary Brunkow et Fred Ramsdell en 2001 ont permis d'identifier la mutation du gène Foxp3 chez la souris. Cette mutation entraînait une perte de fonction des lymphocytes T régulateurs et une forte prédisposition aux maladies auto-immunes graves. Ils ont ensuite établi le lien entre la mutation du gène humain Foxp3 et le syndrome IPEX, une maladie rare mais dévastatrice, confirmant ainsi le rôle indispensable de ce gène dans la régulation immunitaire. Par la suite, Sakaguchi a démontré que Foxp3 est le gène qui gouverne le développement des lymphocytes T régulateurs, unifiant ainsi les découvertes génétiques et cellulaires pour une compréhension complète de la tolérance immunitaire périphérique.
L'Impact Crucial de ces Mécanismes
Le système immunitaire est d'une puissance remarquable, nous protégeant quotidiennement contre des milliers d'agents pathogènes. Cependant, cette puissance nécessite un contrôle précis. Sans régulation, le système immunitaire peut se retourner contre les tissus de l'organisme, provoquant des maladies auto-immunes chroniques et souvent invalidantes, comme le diabète de type 1, la sclérose en plaques et la polyarthrite rhumatoïde. La tolérance immunitaire périphérique, principalement assurée par les lymphocytes T régulateurs, agit comme un « frein » essentiel à cette activité, garantissant l'autotolérance et l'équilibre immunitaire.
Sans ce mécanisme, des interventions médicales vitales courantes, telles que les greffes d'organes, provoqueraient inévitablement un rejet immunitaire. De plus, de nombreuses maladies auto-immunes chroniques resteraient incurables. Les travaux des lauréats ont non seulement approfondi notre savoir scientifique, mais ils ont également catalysé des innovations thérapeutiques majeures, notamment des traitements visant à moduler les lymphocytes T régulateurs pour combattre le cancer, prévenir les troubles auto-immuns et améliorer les résultats des transplantations. Plusieurs thérapies ciblant ces voies sont actuellement en essais cliniques, suscitant un grand espoir pour les patients du monde entier.
Conclusion et Perspectives
Olle Kämpe, président du Comité Nobel, a souligné : « Le travail de Brunkow, Ramsdell et Sakaguchi a été transformateur, révélant les mécanismes complexes et essentiels qui maintiennent l'équilibre du système immunitaire. Leurs découvertes sont fondamentales pour l'immunologie moderne et l'innovation thérapeutique. »
En éclairant les mécanismes par lesquels le système immunitaire protège l'organisme sans s'autodétruire, les lauréats du Prix Nobel 2025 ont fait progresser de manière spectaculaire la biologie fondamentale et la médecine, ouvrant la voie à de meilleurs traitements pour les maladies auto-immunes, le cancer et la transplantation. Cette distinction met en évidence la valeur profonde de la recherche scientifique fondamentale dans le décryptage des systèmes biologiques complexes qui sauvegardent la santé humaine.
45 Vues
Lisez plus d’actualités sur ce sujet :
Avez-vous trouvé une erreur ou une inexactitude ?Nous étudierons vos commentaires dans les plus brefs délais.

