2025年诺贝尔生理学或医学奖:揭示外周免疫耐受机制,开辟自身免疫疾病治疗新路径
作者: Dmitry Drozd

卡罗林斯卡学院诺贝尔大会宣布,将2025年诺贝尔生理学或医学奖授予玛丽·E·布伦科(Mary E. Brunkow)、弗雷德·拉姆斯德尔(Fred Ramsdell)和坂口志文(Shimon Sakaguchi),以表彰他们在“外周免疫耐受”机制研究中取得的开创性发现。外周免疫耐受是防止免疫系统攻击自身组织的关键过程,对于预防自身免疫性疾病至关重要。
免疫学研究的历史脉络与核心挑战
免疫耐受现象——即免疫系统识别并放过自身细胞,同时有效清除有害入侵者的能力——已被研究超过75年。早在1945年,雷·D·欧文(Ray D. Owen)就进行了早期探索。随后,莱斯利·布伦特(Leslie Brent)、鲁珀特·比林厄姆(Rupert Billingham)和彼得·梅达瓦(Peter Medawar)在20世纪50年代的工作奠定了基础,他们证明了免疫系统在特定条件下可以被“训练”接受外来组织。
这些见解催生了“中枢耐受”的概念,即潜在的自我反应性免疫细胞在胸腺发育过程中被清除。伯内特(Burnet)和梅达瓦因“获得性免疫耐受的发现”荣获1960年的诺贝尔奖,认可了这一基本机制。
然而,科学家们逐渐认识到,中枢耐受机制并非完美无缺。一些具有自我反应性的免疫细胞会逃脱胸腺的筛选,继续在体内循环,从而构成自身免疫攻击的潜在风险。正是这一未解之谜,促使玛丽·布伦科、弗雷德·拉姆斯德尔和坂口志文致力于外周耐受的研究,并最终取得了突破。
划时代的细胞与基因发现
在1995年,当许多研究人员仍认为免疫耐受仅依赖于中枢清除机制时,坂口志文发现了一种全新的免疫细胞类型——调节性T细胞(Tregs)。这些细胞在胸腺外部,即外周环境中,积极地抑制针对自身抗原的免疫反应,有效阻止自身免疫性疾病的发生。这一发现揭示了人体存在一种复杂的、持续监控免疫活动的外周机制。
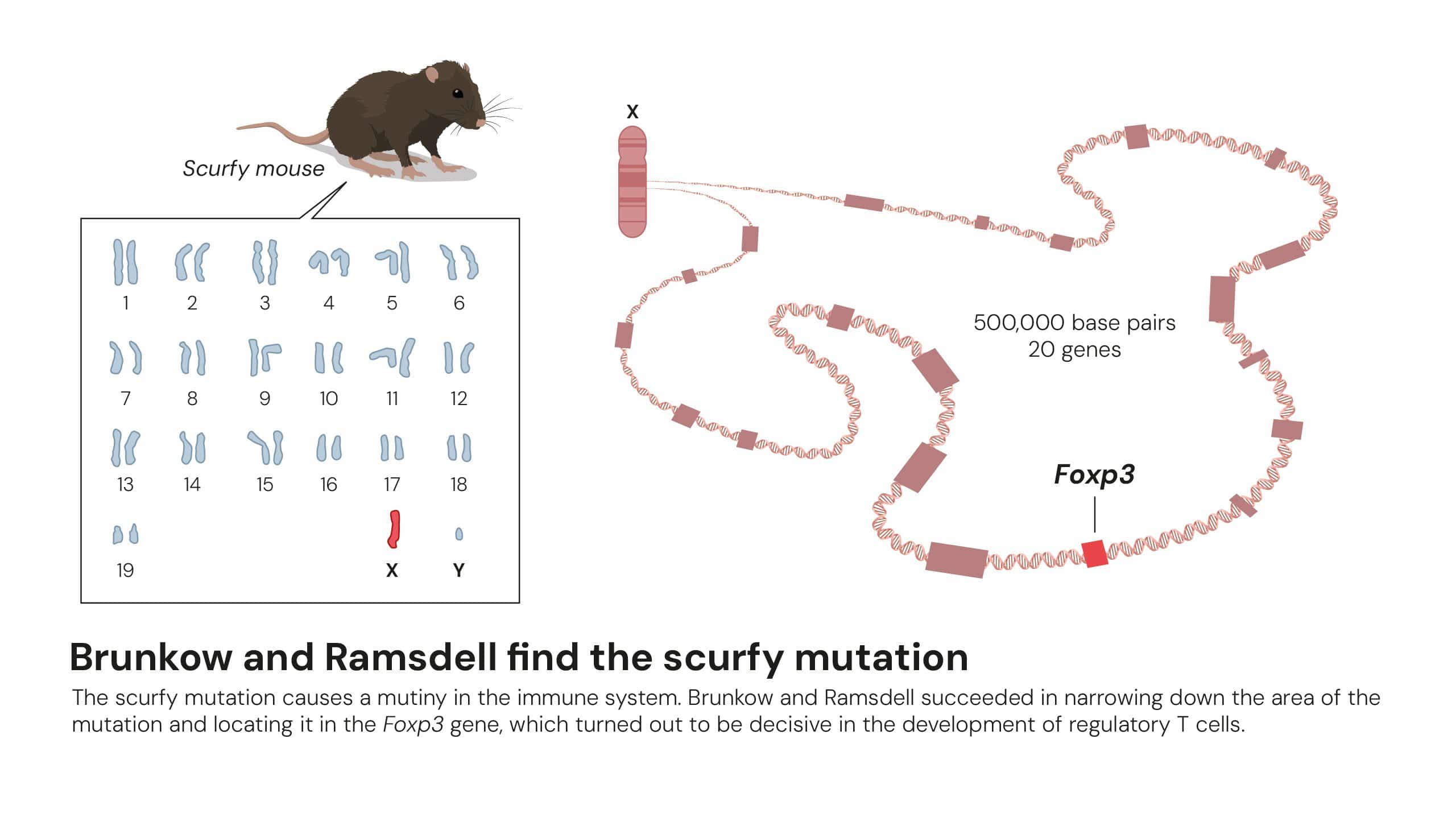
作为对坂口志文发现的有力补充,玛丽·布伦科和弗雷德·拉姆斯德尔于2001年开展了互补研究。他们发现,小鼠体内Foxp3基因突变会导致调节性T细胞功能丧失,并引发严重的自身免疫疾病易感性。他们进一步证实,人类Foxp3基因突变与罕见但破坏性极强的IPEX综合征有关,从而确认了该基因在免疫调节中的核心作用。
随后,坂口志文证明Foxp3基因控制着调节性T细胞的发育,将细胞学和遗传学发现紧密结合,形成了对外周免疫耐受机制的全面理解。
外周免疫耐受为何至关重要
免疫系统拥有强大的力量,每天保护我们免受数千种病原体的侵害。然而,这种力量必须受到精确的控制;否则,免疫系统可能会反过来攻击自身的组织,引发慢性且往往使人衰弱的自身免疫性疾病,例如1型糖尿病、多发性硬化症和类风湿性关节炎。
由调节性T细胞主导的外周免疫耐受机制,正是免疫活动中的关键“刹车片”,确保了自我耐受和免疫平衡的维持。如果没有这种机制,许多挽救生命的医疗干预措施,如器官移植,将必然导致免疫排斥,并且许多慢性自身免疫疾病将无法得到有效治疗。
三位获奖者的发现不仅深化了科学认知,更激发了治疗学的创新浪潮。这些创新包括调节调节性T细胞以对抗癌症、预防自身免疫性疾病以及改善移植结果的疗法。目前,多项针对这些通路的疗法正在临床试验中进行,为全球患者带来了希望。
结语与展望
诺贝尔委员会主席奥勒·坎佩(Olle Kämpe)强调:“布伦科、拉姆斯德尔和坂口志文的工作具有变革性意义,揭示了维持免疫系统平衡的复杂且必要的机制。他们的发现是现代免疫学和治疗学创新的基石。”
通过阐明免疫系统在不自我毁灭的前提下保护身体的机制,这三位2025年诺贝尔奖得主极大地推动了基础生物学和医学的发展,为改善自身免疫性疾病、癌症和移植治疗提供了新的希望。
这一奖项凸显了基础科学研究在揭示保障人类健康的复杂生物系统方面所具有的深远价值。
45 查看
阅读更多关于该主题的新闻:
你发现了错误或不准确的地方吗?我们会尽快考虑您的意见。

